PD Dr. Harun Tüysüz und sein Forschungsteam veröffentlichen neue Erkenntnisse zu frühesten biochemischen Prozessen bei der Entstehung des Lebens in Nature Ecology & Evolution
Ein internationales Forschungsteam aus Deutschland (PD Dr. Harun Tüysüz und Prof. Dr. William Martin), Frankreich (Prof. Dr. Joseph Moran) und Japan (Prof. Dr. Yoichi Kamagata) hat spannende neue Forschungsergebnisse zur Entstehung des Lebens in der Fachzeitschrift Nature Ecology and Evolution publiziert. Im Zentrum der Forschung stehen chemische Prozesse, die an hydrothermalen Tiefseequellen erfolgen und für die Entstehung und den Stoffwechsel von primitivsten Lebensformen nötig sind. Das Forscherteam, dem auch PD Dr. Harun Tüysüz vom Max-Planck-Institut für Kohlenforschung angehört, konnte nachweisen, dass – in Gegenwart von Kohlendioxid als Baustein – Wasserstoff der Treibstoff für die frühesten biochemischen Prozesse am Anfang des Lebens war.
In Laborversuchen stellten die Evolutionsforscher unter der Leitung der HHU Düsseldorf jene Reaktionen nach, die an Tiefseeschloten erfolgen und vermutlich zu den ersten freilebenden Zellen führten. Die Schlote stoßen heißes, mineralhaltiges Wasser aus, das Wasserstoff und Kohlendioxid enthält, welches in einer metallkatalysierten Reaktion Energie für den Stoffwechsel einfachster Lebensformen liefert.
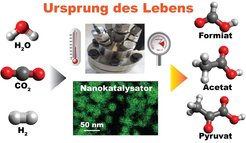
Genauso wie Mikroben sich von Kohlendioxid und Wasserstoffgas ernähren können, dieses in Acetate, Ameisensäure und Pyruvate wandeln und für die Bildung ihres gesamten organischen Materials nutzen, lässt sich die Reaktion im Labor mit Hilfe von passenden Katalysatoren nachstellen. Die Wissenschaftler zeigten, dass sich Wasserstoff H2 und Kohlendioxid CO2 mit einfachen mineralischen Katalysatoren bei 100 °C über Nacht in Acetate, Pyruvate sowie Formiat wandeln lassen. Entscheidend hierfür sind passende nanostrukturierte Feststoffkatalysatoren, die das Team von Harun Tüysüz designte. „Die besondere Struktur unserer Katalysatoren hat die Reaktivität in entscheidendem Maße beeinflusst und vorangetrieben“, erzählt der Forscher.
Die jetzt publizierten Forschungsergebnisse lassen Schlüsse darauf ziehen, wie das Leben entstand. Zunächst gab es einfache chemische Reaktionen, die durch Metalle und Mineralien katalysiert wurden. Aus den Produkten entstanden in den passenden Bedingungen komplexere Nukleinsäuren und Proteine, in denen auch heute noch Relikte der biochemischen Ursprünge nachgewiesen werden können.
Zudem setzen die Reaktionen zwischen dem – auch heute noch – in der Tiefsee gebildeten Wasserstoff und Kohlendioxid Energie frei, die den Stoffwechsel der Urzellen angetrieben haben kann. Wasserstoff ist also nicht nur eine saubere Energiequelle der Zukunft sondern kann – unter den richtigen Bedingungen und in Gegenwart der richtigen Katalysatoren – auch zentral für die Entstehung des Lebens gewesen sein.
Die jetzt publizierte Studie wurde vom Europäischen Forschungsrat, der Volkswagen Stiftung, der Deutschen Forschungsgemeinschaft, der Max-Planck-Gesellschaft, der Japanischen Gesellschaft zur Förderung der Wissenschaften und dem japanischen Ministerium für Bildung, Kultur, Sport, Wissenschaft und Technologie gefördert.












